Weitere Gebrauchsinformationen der Varianten von noristerat
Dieses Präparat ist rezeptpflichtig.
1 Was ist Noristerat und wofür wird es angewendet?
Noristerat ist ein hormonales Empfängnisverhütungsmittel für die intramuskuläre Injektion. Noristerat enthält ein Gelbkörperhormon (Gestagen). Dieses gehört zu der Gruppe der Geschlechtshormone. Noristerat wird angewendet zur Schwangerschaftsverhütung von längerer Dauer (2 - 3 Monate) nur bei Frauen, für die andere Schutzmaßnahmen ungeeignet sind, z. B. wegen gestörter Aufnahme aus dem Magen-Darm-Trakt, wegen Estrogenunverträglichkeit oder unzuverlässiger Anwendung.
2 Was müssen Sie vor der Anwendung von Noristerat beachten?
Noristerat darf nicht angewendet werden, wenn eine der folgenden Bedingungen vorliegt. Sollte eine dieser Bedingungen während der Anwendung von Noristerat auftreten, darf keine weitere Injektion gegeben werden.
Noristerat darf nicht angewendet werden,
- wenn Sie überempfindlich (allergisch) gegen den Wirkstoff oder einen der sonstigen Bestandteile von Noristerat sind,
- bei bestehender oder vermuteter Schwangerschaft,
- bei ungeklärten Blutungen aus der Scheide,
- bei einer bestehenden Blutgerinnselbildung in den Venen (venöse thromboembolische Erkrankung),
- bei vorausgegangenen oder bestehenden arteriellen und Herz-Kreislauf-Erkrankungen (z. B. Herzinfarkt, Schlaganfall, ischämische Herzkrankheit),
- bei krankhaft erhöhtem Blutdruck,
- bei vorangegangenen oder bestehenden schweren Leberkrankheiten mit und ohne Gelbsucht, solange sich die Leberfunktionswerte nicht normalisiert haben,
- bei bekannten oder vermuteten bösartigen Tumoren, die durch Sexualhormone beeinflusst werden (z. B. Tumoren der Geschlechtsorgane, bestehender oder behandelter Brustkrebs oder Gebärmutterkrebs),
- bei Diabetes mit Gefäßveränderungen,
- bei vorausgegangenen oder bestehenden Lebertumoren (gutoder bösartig),
- bei Fettstoffwechselstörungen.
Noristerat sollte nur nach sorgfältiger Nutzen-Risiko-Abwägung angewendet werden
- in der Stillzeit, insbesondere während der ersten 6 Wochen (geringe Mengen des Wirkstoffs gehen in die Muttermilch über),
- bei Extrauteringravidität (Schwangerschaft außerhalb der Gebärmutter) in der Vorgeschichte,
- bei Vorhandensein nur eines Eileiters,
- bei Porphyrie (einer bestimmten Stoffwechselkrankheit, die einen Blutbestandteil betrifft),
- bei allen Formen eingeschränkter Leberfunktion,
- bei vorausgegangener Blutpfropfbildung (thromboembolische Krankheiten, z. B. tiefen Venenthrombosen, Lungenembolie) sowie Zuständen, die die Anfälligkeit für eine Blutpfropfbildung (z. B. tiefe Venenthrombosen, Lungenembolie, Hirnschlag, Herzinfarkt) erhöhen.
Von einer erneuten Injektion ist abzusehen, wenn während der Anwendung auftreten:
- erstmalig migräneartige oder häufiger ungewohnt starke Kopfschmerzen,
- plötzliche Empfindungs-, Wahrnehmungsstörungen (Seh-, Hörstö- rungen) sowie Bewegungsstörungen, insbesondere Lähmungen (mögliche erste Anzeichen eines Schlaganfalls),
- ungewohnte Schmerzen oder Schwellungen in den Beinen, stechende Schmerzen beim Atmen oder Husten unklarer Ursache, Schmerz- und Engegefühl im Brustraum. (Es könnte sich in diesen Fällen um eine Blutpfropfbildung handeln.)
- Gelbsucht,
- Juckreiz am ganzen Körper,
- Zunahme epileptischer Anfälle,
- stärkerer Blutdruckanstieg,
- Depressionen, die nicht auf äußere Einflüsse zurückzuführen sind,
- krankhafte Veränderungen der Leberfunktion und der Hormonspiegel.
Dasselbe gilt für den Fall, dass der Verdacht einer Schwangerschaft besteht (z. B. bedingt durch die gleichzeitige Anwendung anderer Medikamente, siehe „Bei Anwendung von Noristerat mit anderen Arzneimitteln“). Über den Schwangerschaftsverdacht ist mit dem Arzt zu sprechen.
Besondere Vorsicht bei der Anwendung von Noristerat ist erforderlich,
Nur Frauen mit normalem Zyklusverlauf dürfen Noristerat erhalten.
Gynäkologische und allgemeine Untersuchungen
Vor der Anwendung soll eine gründliche allgemeine sowie gynäkologische Untersuchung (einschließlich der Brust und eines zytologischen Zervixabstrichs) durchgeführt und eine Schwangerschaft ausgeschlossen werden.
Während der Anwendung sind zunächst nach 2 Monaten und später in halbjährlichen Abständen die allgemeine und gynäkologische Untersuchung zu wiederholen, um unerwünschte Wirkungen (siehe 4. „Welche Nebenwirkungen sind möglich?“) frühzeitig erfassen zu können.
Brustkrebs
In Studien zeigte sich kein erhöhtes Brustkrebsrisiko für Frauen, die jemals Verhütungsmittel in Form von Depotspritzen wie Noristerat angewendet hatten, im Vergleich zu Frauen, die niemals Verhütungsmittel in Form von Depotspritzen angewendet hatten. Allerdings wurde ein erhöhtes Risiko in bestimmten Untergruppen gefunden, unter anderem für Frauen, die Verhütungsmittel in Form von Depotspritzen erstmals in den letzten fünf Jahren vor Ihrer Brustkrebsdiagnose angewendet hatten. Es ist möglich, dass ein Brustkrebs in einem sehr frühen Stadium durch Gabe von Noristerat zu einem weiteren Wachstum angeregt wird.
Zur Beachtung:
Aufgrund des Gehaltes an Benzylbenzoat können bei entsprechend veranlagten Patienten Überempfindlichkeitsreaktionen in Form von Reizungen an Haut, Augen und Schleimhäuten auftreten. Bei Neugeborenen besteht ein erhöhtes Auftreten von Gelbsucht.
Androgene Restwirkung (Wirkung männlicher Geschlechtshormone)
Das in Noristerat enthaltene Norethisteronenantat hat im Tierversuch eine androgene Restwirkung (siehe auch 4. „Welche Nebenwirkungen sind möglich?“), die jedoch bei empfohlener Dosierung nur äußerst selten in Erscheinung tritt. Es gibt aber Frauen mit besonderer Empfindlichkeit gegenüber androgenen Impulsen, ohne dass hierfür sichere Anzeichen erkennbar wären. Daher kann es in Einzelfällen zu leichten Vermännlichungserscheinungen kommen.
Im Zusammenhang mit der androgenen Restwirkung von Estranderivaten sind in früheren Jahren, als diese Substanzen in sehr hoher Dosierung zur Schwangerschaftserhaltung angewendet wurden, auch nach Gabe norethisteronhaltiger Präparate einzelne Fälle von Vermännlichung der äußeren Geschlechtsmerkmale weiblicher Neugeborener beschrieben worden. Bei den wenigen Schwangerschaften, zu denen es bisher während des Abklingens der Noristerat-Wirkung gekommen ist, wurde ein solcher Effekt jedoch nicht beobachtet.
Noristerat und Thrombose
Unter einer Thrombose/Thromboembolie wird die Bildung eines Blutgerinnsels (Blutpfropf) verstanden, das ein Blutgefäß verschließen kann.
Thrombosen treten unter anderem in den tiefen Venen der Beine auf (tiefe Beinvenenthrombose). Wenn sich ein solches Blutgerinnsel löst, kann es mit dem Blutstrom in die Lungenarterien gelangen und dort ein Blutgefäß verschließen (Lungenembolie).
Einige neuere Studien weisen darauf hin, dass die Anwendung von Pillen, die nur ein Gelbkörperhormon (Gestagen) enthalten, das Risiko für venöse Thrombosen erhöhen könnte. Als allgemein anerkannte Risikofaktoren für venöse Thrombosen gelten
- eine venöse Blutpfropfbildung in der eigenen Krankengeschichte oder bei Familienangehörigen (bei Geschwistern oder Eltern in relativ jungen Jahren),
- Alter,
- Fettleibigkeit (Adipositas),
- länger andauernde Immobilisierung, größere Operationen oder größere Verletzungen.
Im Falle einer längerfristigen Immobilisierung ist es ratsam, die Anwendung von Noristerat zu unterbrechen (bei Wahlmöglichkeit eines Operationstermins zwölf Wochen im Voraus) und erst zwei Wochen nach vollständiger Remobilisierung fortzusetzen. Wenn möglich, sollte besonders bei Frauen mit bekannten Risikofaktoren für eine Blutpfropfbildung, bei Bauchoperationen und Operationen der unteren Gliedmaße auf die rechtzeitige Unterbrechung der Noristerat-Anwendung geachtet werden.
Das erhöhte Risiko für eine Thromboembolie kurz nach einer Geburt ist ebenfalls zu berücksichtigen (siehe auch Abschnitt „Schwangerschaft und Stillzeit“).
Eine Thrombose kann auch in einer Schlagader auftreten (arterielle Thrombose), z. B. in den Herzkranzgefäßen (Koronararterien) oder den hirnversorgenden Arterien und so zu einem Herzinfarkt bzw. Schlaganfall führen.
Aus wissenschaftlichen Studien liegen wenige Beweise für einen Zusammenhang zwischen der Anwendung von Pillen, die nur ein Gelbkörperhormon (Gestagen) enthalten, und einem erhöhten Risiko für Herzinfarkt und Schlaganfall vor. Das Risiko für solche Ereignisse steht eher in Verbindung mit zunehmendem Alter, Bluthochdruck und Rauchen. Für Frauen mit Bluthochdruck kann das Schlaganfall-Risiko durch die Anwendung reiner Gestagen-Präparate wie Noristerat leicht erhöht sein.
Wenn Sie mögliche Anzeichen einer Thrombose bemerken (siehe „Von einer erneuten Injektion ist abzusehen, wenn während der Anwendung auftreten:“), suchen Sie unverzüglich einen Arzt auf.
Zyklusverlauf
Während der Behandlung mit Noristerat kann es zu individuell unterschiedlichen Störungen im Zyklusverlauf kommen. Diese Begleiterscheinung ist nur selten ein Anlass zum Absetzen von Noristerat.
Zyklische Blutungen:
Der Anteil der Frauen, bei denen sich der Zyklus nicht deutlich verändert (Blutungsintervalle zwischen 26 und 35 Tage, Blutungsdauer 1 - 7 Tage), liegt bei 50 - 70 %. Mit fortschreitender Anwendungsdauer besteht eine Tendenz zur Stabilisierung des Zyklus.
Zwischenblutungen:
Zwischenblutungen können entweder den Charakter von Schmierblutungen haben oder in Menstruationsstärke auftreten. Aus medizinischer Sicht besteht kein Anlass, Noristerat abzusetzen. Sie sollten jedoch Ihren Arzt informieren, damit organische Ursachen derartiger Blutungen ausgeschlossen werden können.
Ausbleiben der monatlichen Regelblutung (Amenorrhö):
Während der mehrjährigen klinischen Prüfung kam es bei 8 - 25 % der Frauen zu Amenorrhöen, die im Allgemeinen von kurzer Dauer waren und im Verlauf der weiteren Anwendung verschwanden. Die Amenorrhörate nahm bei längerer Anwendung von Noristerat nicht zu.
Leber
Nach einer viralen Leberentzündung kann Noristerat angewendet werden, sobald die Leberfunktionsparameter wieder normal sind.
Einfluss auf den Kohlenhydratstoffwechsel (Zuckerstoffwechsel)
Gelbkörperhormone (Gestagene) können abhängig von Art und Menge vor allem bei erhöhtem Zuckerkonsum zu einer verminderten Zuckertoleranz führen. Die Veränderungen sind im Allgemeinen nach dem Absetzen reversibel. Da der Einfluss auf den Kohlenhydratstoffwechsel nicht voraussehbar ist, sollten Frauen mit Diabetes mellitus (Zuckerkrankheit) oder Neigung dazu, auch diejenigen mit Diabetes mellitus während einer vorangegangenen Schwangerschaft, sorgfältig überwacht werden. Der Bedarf an Insulin oder Arzneimitteln gegen Diabetes mellitus kann sich sowohl erhöhen als auch verringern.
Verlust an Knochendichte
Bei der Anwendung von Noristerat kann es zu einer Verringerung der Knochendichte und zu einem verminderten Aufbau der Spitzenknochenmasse kommen. Dieser Verlust an Knochendichte ist in der Jugend und dem frühen Erwachsenenalter von besonderer Bedeutung, da dies eine entscheidende Phase für den Knochenzuwachs ist.
Noristerat sollte zur Empfängnisverhütung über einen längeren Zeitraum (z. B. länger als 2 Jahre) daher nur dann angewendet werden, wenn andere Verhütungsmethoden nicht angezeigt sind. Wenn bei Ihnen bereits ein erhöhtes Risiko für eine verminderte Knochendichte besteht (fragen Sie dazu Ihren Arzt), kann die Noristerat-Behandlung dieses Risiko weiter erhöhen. In diesem Fall sollten Sie andere Verhütungsmethoden in Betracht ziehen. Bei langfristiger Anwendung von Noristerat sollte in regelmäßigen Abständen die Knochendichte überprüft werden. Sie sollten darauf achten, ausreichende Mengen an Kalzium- und Vitamin-D zuzuführen, falls keine anderen Gründe dagegen sprechen.
Sonstiges
Geringe Blutdruckanstiege wurden bei Frauen, die „kombinierte Pillen“ (mit zwei hormonalen Wirkstoffen) einnahmen, sowie bei Frauen, die im Rahmen einer Studie injizierbare Verhütungsmittel erhielten, berichtet. Wenn sich während der Anwendung von Noristerat ein anhaltender Bluthochdruck entwickelt oder ein Anstieg des Blutdrucks durch blutdrucksenkende Medikamente nicht ausreichend zu behandeln ist, sollte Noristerat abgesetzt werden.
Folgende Erkrankungen können sowohl in der Schwangerschaft als auch bei Anwendung der Pille auftreten oder sich verschlimmern. Dies sollte bei der Anwendung von Verhütungsmitteln, die nur eine Gelbkörperhormon enthalten, in Betracht gezogen werden.
- Gelbsucht und/oder Juckreiz in Verbindung mit Gallenstauung,
- Bildung von Gallensteinen,
- Schmetterlingsflechte (systemischer Lupus erythematodes, eine bestimmte Autoimmunkrankheit),
- hämolytisch-urämisches Syndrom (eine bestimmte Erkrankung des Blutes),
- Chorea Sydenham (eine bestimmte Erkrankung des zentralen Nervensystems).
Das erneute Auftreten von Gelbsucht oder Juckreiz in Verbindung mit einer Gallenstauung, welche zuerst während einer Schwangerschaft oder bei früherer Anwendung von Sexualhormonen aufgetreten sind, erfordert eine Unterbrechung der Noristerat-Anwendung.
Gelblichbraune Pigmentflecken (Chloasmen) können gelegentlich auftreten, besonders bei Frauen, bei denen solche Pigmentflecken während einer früheren Schwangerschaft aufgetreten sind. Frauen mit einer Veranlagung zu Chloasmen sollten während der Anwendung von Noristerat direktes Sonnenlicht oder ultraviolette Strahlung meiden.
Wenn während der Behandlung früher aufgetretene Depressionen erneut auftreten, sollte keine weitere Injektion gegeben werden.
Bitte beachten Sie, dass Noristerat nicht vor HIV-Infektionen (AIDS) und anderen sexuell übertragbaren Krankheiten schützt.
Verminderte Wirksamkeit
Die Wirksamkeit von Noristerat kann im Falle eines verlängerten Injektionsintervalls (siehe 3. „Wie ist Noristerat anzuwenden?“) oder bei begleitender Medikation (siehe „Bei Anwendung von Noristerat mit anderen Arzneimitteln“) vermindert sein.
Bei Anwendung von Noristerat mit anderen Arzneimitteln:
Bitte informieren Sie Ihren Arzt oder Apotheker, wenn Sie andere Arzneimittel einnehmen/anwenden bzw. vor kurzem eingenommen/angewendet haben, auch wenn es sich um nicht verschreibungspflichtige Arzneimittel handelt.
Wechselwirkungen
Es sind keine Daten zu Wechselwirkungen von Injektionspräparaten wie Noristerat, die nur ein Gelbkörperhormon enthalten, mit anderen Arzneimitteln bekannt. Die folgenden Wechselwirkungen basieren auf Erfahrungen mit „kombinierten Pillen“.
Verschiedene Substanzen, z. B. Barbituarate, Phenylbutazon, Rifampicin, Rifabutin, bestimmte Arzneimittel gegen Epilepsie (wie Barbexaclon, Carbamazepin, Oxcarbazepin, Phenytoin, Primidon) und Präparate, die Johanniskraut (Hypericum perforatum) enthalten, sowie vermutlich auch Griseofulvin, können durch die Aktivierung von Leberenzymen den Abbau von Norethisteron verstärken und die empfängnisverhütende Wirkung von Noristerat beeinträchtigen. Das Auftreten von Schmierblutungen kann ein erster Hinweis auf solche Vorgänge sein.
Auch einige Arzneimittel gegen Infektionen (Ampicillin, Tetracyclin) können die Wirksamkeit vermindern.
Hormonale Verhütungsmittel können auch den Stoffwechsel anderer Arzneimittel beeinträchtigen. Infolgedessen können Plasma- und Gewebekonzentrationen dieser Arzneimittel beeinflusst werden (z. B. von Ciclosporin).
Auch ist es möglich, dass sich der Bedarf an Arzneimitteln gegen Diabetes (mellitus) ändert.
Laboruntersuchungen
Die Anwendung von hormonalen Verhütungsmitteln kann die Ergebnisse bestimmter Labortests beeinflussen.
Schwangerschaft und Stillzeit
Noristerat darf in der Schwangerschaft nicht angewendet werden (siehe „Noristerat darf nicht angewendet werden“). Vor Beginn der Behandlung muss das Bestehen einer Schwangerschaft ausgeschlossen werden.
Noristerat sollte in der Stillzeit nicht angewendet werden, da Norethisteron in die Muttermilch übergeht. Hormonale Verhütungsmittel, die nur ein Gelbkörperhormon enthalten, gelten aber als nächstbeste Wahl nach nicht-hormonalen Verhütungsmethoden. Es scheinen keine ungünstigen Wirkungen auf das Wachstum oder die Entwicklung des Säuglings aufzutreten, wenn Verhütungsmittel, die nur ein Gelbkörperhormon enthalten, ab sechs Wochen nach der Geburt angewendet werden.
Fragen Sie vor der Einnahme/Anwendung von allen Arzneimitteln Ihren Arzt oder Apotheker um Rat.
Verkehrstüchtigkeit und das Bedienen von Maschinen:
Es sind keine besonderen Vorsichtsmaßnahmen erforderlich.
3 Wie ist Noristerat anzuwenden?
Art der Anwendung:
Ölige Lösungen wie Noristerat sind ausschließlich tief intramuskulär zu injizieren (vorzugsweise in den Gesäßmuskel, alternativ auch in den Oberarm); insbesondere ist eine Injektion in Blutgefäße zu vermeiden. Die in Einzelfällen während oder unmittelbar nach der Injektion öliger Lösungen auftretenden kurzdauernden Reaktionen (Hustenreiz, Hustenanfälle, Atemnot) lassen sich erfahrungsgemäß durch betont langsames Injizieren vermeiden.
Es empfiehlt sich, die Einspritzstelle anschließend mit einem Pflaster zu versehen, damit die Lösung nicht zurückfließen kann.
Beginn der Anwendung:
- Keine vorangegengene Anwendung von hormonalen Verhütungsmitteln
Die erste intramuskuläre Injektion wird innerhalb der ersten fünf Tage eines Zyklus vorgenommen, d. h. in den ersten fünf Tagen der Menstruationsblutung. Der Empfängnisschutz beginnt bei vorschriftsgemäßer Anwendung am Tag der ersten Injektion. - Wechsel von einer „kombinierten Pille“ (mit zwei hormonalen Wirkstoffen)
Vorzugsweise sollte sofort am Tag nach der letzten wirkstoffhaltigen Tablette der bisher verwendeten „kombinierten Pille“ mit Noristerat begonnen werden. Bei einem späteren Beginn sollte während der ersten sieben Tage nach der Injektion zusätzlich eine Barrieremethode (z. B. ein Kondom) zur Verhütung angewendet werden. - Wechsel von einem Gestagenmonopräparat (Minipille, Injektion, Implantat) oder einem Gestagen-freisetzenden Intrauterinpessar:
Von der Minipille kann jederzeit ohne Unterbrechung zu Noristerat gewechselt werden; (von einem Implantat oder einem Intrauterinpessar am Tag der Entfernung; von einem anderen Injektionspräparat, wenn die nächste Injektion fällig wäre). In jedem Fall sollte jedoch während der ersten sieben Tage nach der Injektion zusätzlich eine Barrieremethode (z. B. ein Kondom) zur Verhütung angewendet werden. - Nach einer Fehlgeburt oder einer Entbindung:
Noristerat kann sofort nach einer Fehlgeburt oder einer Entbindung angewendet werden, solange keine ärztlichen Bedenken vorliegen (zur Stillzeit siehe „Schwangerschaft und Stillzeit“).
Folgeinjektionen:
Die nächsten drei Spritzen sind unabhängig vom Blutungsmuster in Abständen von jeweils 8 Wochen zu verabreichen.
Danach ist alle 12 Wochen (84 Tage) eine weitere Injektion erforderlich. Anderenfalls besteht von der 13. Woche an kein ausreichender Schutz mehr vor einer Schwangerschaft.
Unter besonderen Umständen (z. B. Reisen, Feiertage) kann der Abstand zwischen den Spritzen um eine Woche verkürzt werden.
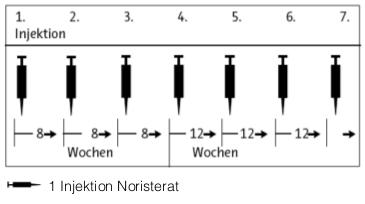
Die jeweils nächste Injektion soll nur dann gegeben werden, wenn es innerhalb der letzten 8 - 12 Wochen zu einer menstruationsähnlichen Blutung gekommen ist. Sonst muss vor einer erneuten NoristeratInjektion eine Schwangerschaft ausgeschlossen werden.
Dauer der Anwendung:
Noristerat kann - ähnlich wie orale Kontrazeptiva - über mehrere Jahre angewendet werden.
Bitte sprechen Sie mit Ihrem Arzt oder Apotheker, wenn Sie den Eindruck haben, dass die Wirkung von Noristerat zu stark oder zu schwach ist.
Wenn Sie eine größere Menge Noristerat angewendet haben, als Sie sollten
Es liegen keine Berichte ernsthafter gesundheitsschädlicher Wirkungen aufgrund einer Überdosierung vor. Es sind keine Gegenmittel bekannt. Die Behandlung sollte sich an den Symptomen orientieren.
Wenn Sie weitere Fragen zur Anwendung des Arzneimittels haben, fragen Sie Ihren Arzt oder Apotheker.
4 Welche Nebenwirkungen sind möglich?
Wie alle Arzneimittel kann Noristerat Nebenwirkungen haben, die aber nicht bei jedem auftreten müssen.
Bei der Bewertung von Nebenwirkungen werden folgende Häufigkeitsangaben zugrunde gelegt:
| Sehr häufig: mehr als 1 von 10 Behandelten Häufig: weniger als 1 von 10, aber mehr als 1 von 100 Behandelten Gelegentlich: weniger als 1 von 100, aber mehr als 1 von 1000 Behandelten Selten: weniger als 1 von 1000, aber mehr als 1 von 10 000 Behandelten Sehr selten: weniger als 1 von 10 000 Behandelten, einschließlich Einzelfälle |
Die schwerwiegendsten Nebenwirkungen, die mit dem Gebrauch hormonaler Verhütungsmittel in Verbindung gebracht werden, sind im Abschnitt „Besondere Vorsicht bei der Anwendung von Noristerat ist erforderlich“ aufgeführt. Andere Nebenwirkungen, die von Noristerat-Anwenderinnen berichtet wurden (Daten nach Inverkehrbringen), sind:
| Systemorganklasse | Sehr häufig | Häufig | Gelegentlich |
| Erkrankungen des Immunsystem | Überempfindlichkeitsreaktionen | ||
| Psychiatrische Erkrankungen | Nervosität; Depressive Verstimmungen | ||
| Erkrankungen des Nervensystem | Kopfschmerzen; Schwindelgefühl | ||
| Erkrankungen des Magen-Darm-Traktes | Übelkeit | ||
| Erkrankungen der Haut und des Unterhautzellgewebes | verschiedene Hautbeschwerden | Akne; lokale Hautreaktionen | |
| Erkrankungen der Geschlechtsorgane und der Brustdrüse | Blutungen aus der Scheide, einschließlich Schmierblutungen und Zwischenblutungen unterschiedlicher Stärke; Ausbleiben der monatlichen Regelblutung (Amenorrhöen), übermäßig starke Regelblutung (Hypermenorrhöen) und unregelmä- ßige Zyklen | ||
| Allgemeine Erkrankungen und Beschwerden am Verabreichungsort | Reaktionen an der Injektionsstelle | ||
| Stoffwechselund Ernährungsstörungen | Gewichtszunahme |
Erkrankungen der Atemwege, des Brustraums und Mediastinums Die in Einzelfällen während oder unmittelbar nach der Injektion öliger Lösungen auftretenden kurzdauernden Reaktionen (Hustenreiz, Hustenanfälle, Atemnot) lassen sich erfahrungsgemäß durch betont langsames Injizieren vermeiden.
Selten können Überempfindlichkeitsreaktionen durch Benzylalkohol auftreten.
Nach Absetzen von Noristerat kann bis zu einem halben Jahr vergehen, bis es wieder regelmäßig zum Eisprung kommt.
Wenn die Anwendung wegen Ausbleibens von Blutungen abgebrochen worden ist (siehe auch „Besondere Vorsicht bei der Anwendung von Noristerat ist erforderlich“), sind weitere diagnostische Maßnahmen zur Klärung der Ursachen notwendig. Liegt keine Schwangerschaft vor, und hält die Amenorrhö weiter an, ist besonders bei jüngeren Frauen eine Spezialbehandlung erforderlich.
Diabetikerinnen und Frauen, die zu Diabetes (mellitus) neigen, sollten sorgfältig beobachtet werden (Glucosetoleranz überprüfen), weil während der Anwendung von Gestagenen in einigen Fällen eine Verminderung der Glucosetoleranz festgestellt wurde.
In Einzelfällen können bei Frauen mit besonderer Empfindlichkeit gegenüber androgenen Impulsen Stimmveränderungen auftreten. Besonders bei Frauen mit Sing- oder Sprechberufen ist zu erwägen, ob die Behandlung bei den ersten Anzeichen von Stimmveränderungen (leichte Ermüdbarkeit der Stimme, Rauhigkeit, Heiserkeit) beendet werden sollte.
In seltenen Fällen sind nach Anwendung von Geschlechtshormonen gutartige, noch seltener bösartige Veränderungen an der Leber beobachtet worden, die vereinzelt zu lebensgefährlichen Blutungen in die Bauchhöhle geführt haben. Deshalb ist der Arzt zu informieren, wenn ungewohnte Oberbauchbeschwerden auftreten, die nicht von selbst bald vorübergehen.
Sollten unbekannte Schmerzen im Unterbauch in Verbindung mit einem unregelmäßigen Zyklusmuster auftreten (vor allem ein Ausbleiben der monatlichen Regelblutung gefolgt von Dauerblutungen), muss eine Bauchhöhlenschwangerschaft in Erwägung gezogen werden.
Nach dem gegenwärtigen Erkenntnisstand kann ein Zusammenhang zwischen der Anwendung hormonaler Kontrazeptiva und einem erhöhten Risiko für venöse und arterielle thromboembolische Erkrankungen nicht ausgeschlossen werden. Das relative Risiko für arterielle Thrombosen (Schlaganfall, Herzinfarkt) scheint sich bei einem Zusammentreffen von starkem Rauchen, steigendem Lebensalter und der Anwendung hormonaler Kontrazeptiva weiter zu erhöhen.
Geringe Blutdruckanstiege wurden bei Frauen, die „kombinierte Pillen“ (mit zwei hormonalen Wirkstoffen) einnahmen, sowie bei Frauen, die im Rahmen einer Studie injizierbare Verhütungsmittel erhielten, berichtet. Wenn sich während der Anwendung von Noristerat ein anhaltender Bluthochdruck entwickelt oder ein Anstieg des Blutdrucks durch blutdrucksenkende Medikamente nicht ausreichend zu behandeln ist, sollte Noristerat abgesetzt werden.
Nach Markteinführung wurden bei der Anwendung von Verhütungsmitteln in Form von Depotspritzen Fälle von Brustkrebs berichtet (siehe Abschnitt „Was müssen Sie vor der Anwendung von Noristerat beachten?“).
Bei der Anwendung von Verhütungsmittel in Form von Depotspritzen, wie z. B. Noristerat, kann es zu einer Verminderung der Knochendichte kommen (siehe Abschnitt „Was müssen Sie vor der Anwendung von Noristerat beachten?“).
Informieren Sie bitte Ihren Arzt oder Apotheker, wenn einer der aufgeführten Nebenwirkungen Sie erheblich beeinträchtigt oder Sie Nebenwirkungen bemerken, die nicht in dieser Gebrauchsinformation angegeben sind.
5 Wie ist Noristerat aufzubewahren?
Arzneimittel für Kinder unzugänglich aufbewahren.
Sie dürfen das Arzneimittel nach dem auf dem Umkarton/Behältnis nach „Verwendbar bis“ angegebenen Verfallsdatum nicht mehr verwenden.
Aufbewahrungsbedingungen:
Ampulle im Umkarton aufbewahren, um den Inhalt vor Licht zu schützen.
6 Weitere Informationen
Was Noristerat enthält:
Der Wirkstoff ist Norethisteronenantat.
1 ml enthält 200 mg Norethisteronenantat in öliger Lösung.
Die sonstigen Bestandteile sind:
Benzylbenzoat und Rizinusöl für Injektionszwecke
Inhalt der Packung:
Ampulle zu 1 ml
Pharmazeutischer Unternehmer und Importeur
Einfuhr, Umpackung und Vertrieb:
kohlpharma GmbH, Im Holzhau 8, 66663 Merzig
Diese Gebrauchsinformation wurde zuletzt überarbeitet im April 2009.
Eigenschaften
Die Wirkung von Noristerat beruht in erster Linie auf einer sich über die gesamte Dauer der Anwendung erstreckenden Veränderung des Schleims im Gebärmutterhals, so dass der männliche Samen nicht weit genug vordringen kann. Hormonuntersuchungen haben weiterhin gezeigt, dass innerhalb der ersten 5 - 7 Wochen nach der Injektion die Eireifung durch den hohen Plasmaspiegel von Norethisteron unterdrückt wird. Außerdem ist die Schleimhaut der Gebärmutter für den Beginn einer Schwangerschaft unzureichend vorbereitet.
Im Rahmen klinischer Studien hat man Noristerat im Allgemeinen in Abständen von 12 Wochen injiziert. Die empfängnisverhütende Zuverlässigkeit lag im Vergleich mit oralen Gestagen-Estrogen-Präparaten (so genannte „Pille“) niedriger. Die Mehrzahl der beobachteten Schwangerschaften trat innerhalb der ersten beiden Injektionsintervalle auf. Bei einer längeren Anwendungsdauer zeigte sich auch eine deutlich bessere kontrazeptive Zuverlässigkeit. Darüber hinaus stellte man fest, dass sich durch die Gabe von Noristerat in Abständen von acht Wochen zu Beginn der Behandlung die kontrazeptive Wirkung verbesserte.
Besondere Hinweise
Noristerat beeinträchtigt nicht die Quantität und Qualität der Milchproduktion bei stillenden Frauen. Es wurden auch bisher keine ungünstigen Wirkungen auf Brustkinder beobachtet. Allerdings können geringe Mengen des Steroids mit der Milch ausgeschieden werden. Wie bei anderen Steroiden besteht deshalb besonders in der ersten Lebenswoche die theoretische Möglichkeit, dass der Bilirubinabbau des Neugeborenen beeinflusst wird. Ist bei starker oder länger anhaltender Neugeborenengelbsucht eine ärztliche Behandlung des Kindes erforderlich, muss das Stillen unterbrochen werden.
Ausführlichere Informationen zum Präparat, die der Arzt benötigt, sind in speziellen Druckschriften enthalten.
Kohlpharma GmbH
7 Preisvergleich - Noristerat 200mg kohlpharma Injektionslösung
Noristerat 200mg kohlpharma Injektionslösung Preisvergleich
Für den Kauf empfehlen wir Ihnen den Apothekenpreisvergleich Sparmedo.de. Dort werden die Preise von über 70 zertifizierten Versandapotheken verglichen, wodurch Noristerat 200mg kohlpharma Injektionslösung günstig bestellt werden kann.
Preise vergleichen